实验室围绕玫瑰痤疮与化脓性汗腺炎、毛发疾病与再生、皮肤衰老三大方向,开展从分子机制到临床干预的系统性研究。
玫瑰痤疮与化脓性汗腺炎
玫瑰痤疮是一种严重影响生活质量的慢性炎症性皮肤病,其发病机制尚未完全阐明。实验室建立了涵盖代谢组学、单细胞转录组学、神经源性信号与遗传学的综合研究体系,从多个维度系统揭示该疾病的发病机制。
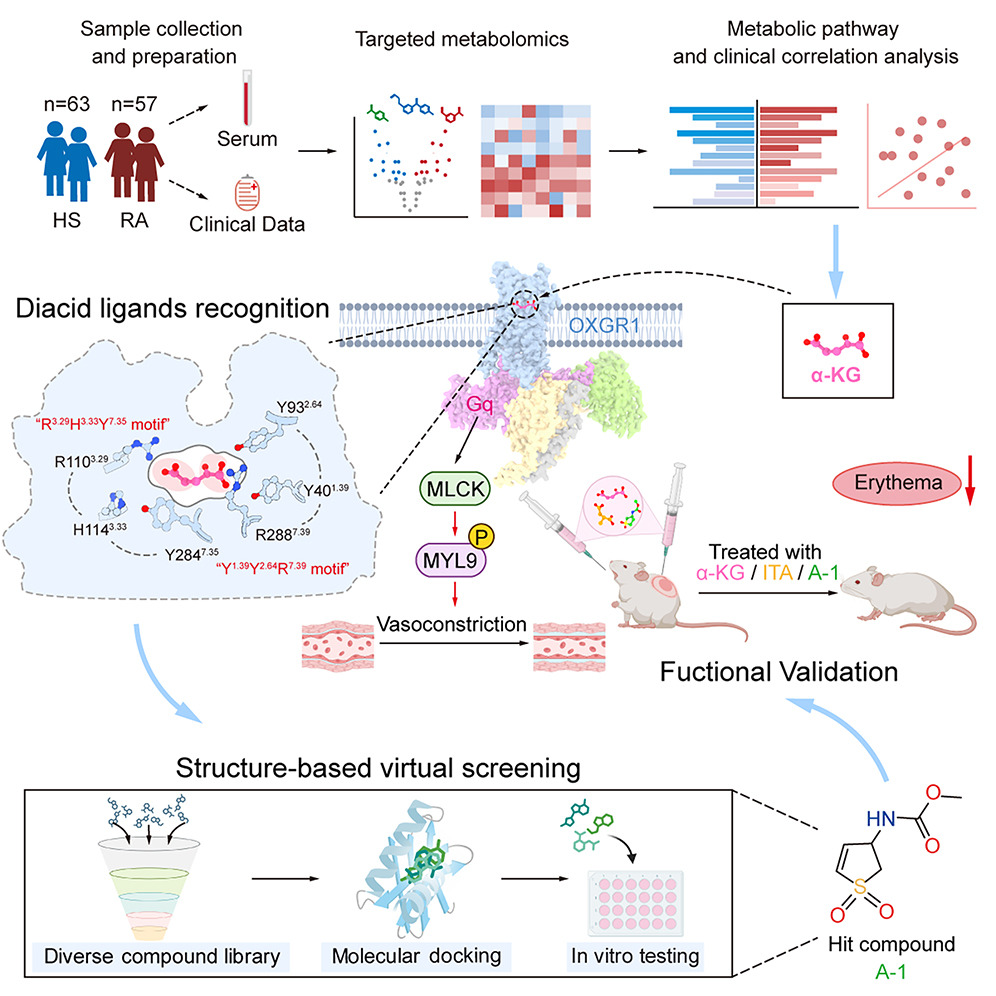
团队发现 α-酮戊二酸(α-KG)是玫瑰痤疮相关代谢物,可激活血管平滑肌细胞表面受体 OXGR1,促进血管收缩并抑制病理性血管扩张。基于 OXGR1-Gq 复合物的冷冻电镜结构,开发了选择性激动剂 A-1,其改善红斑的疗效与一线治疗相当(Cell 2026)。在细胞水平,单细胞转录组学揭示促炎成纤维细胞是玫瑰痤疮病变中血管扩张信号的主要来源,敲除 PTGDS 可抑制小鼠模型中的疾病表型进展(Nat Commun 2024)。此外,团队证实感觉神经元通过 CGRP-RAMP1 轴激活 γδ T 细胞,揭示了介导面部超敏反应的神经免疫回路(Nat Commun 2024)。
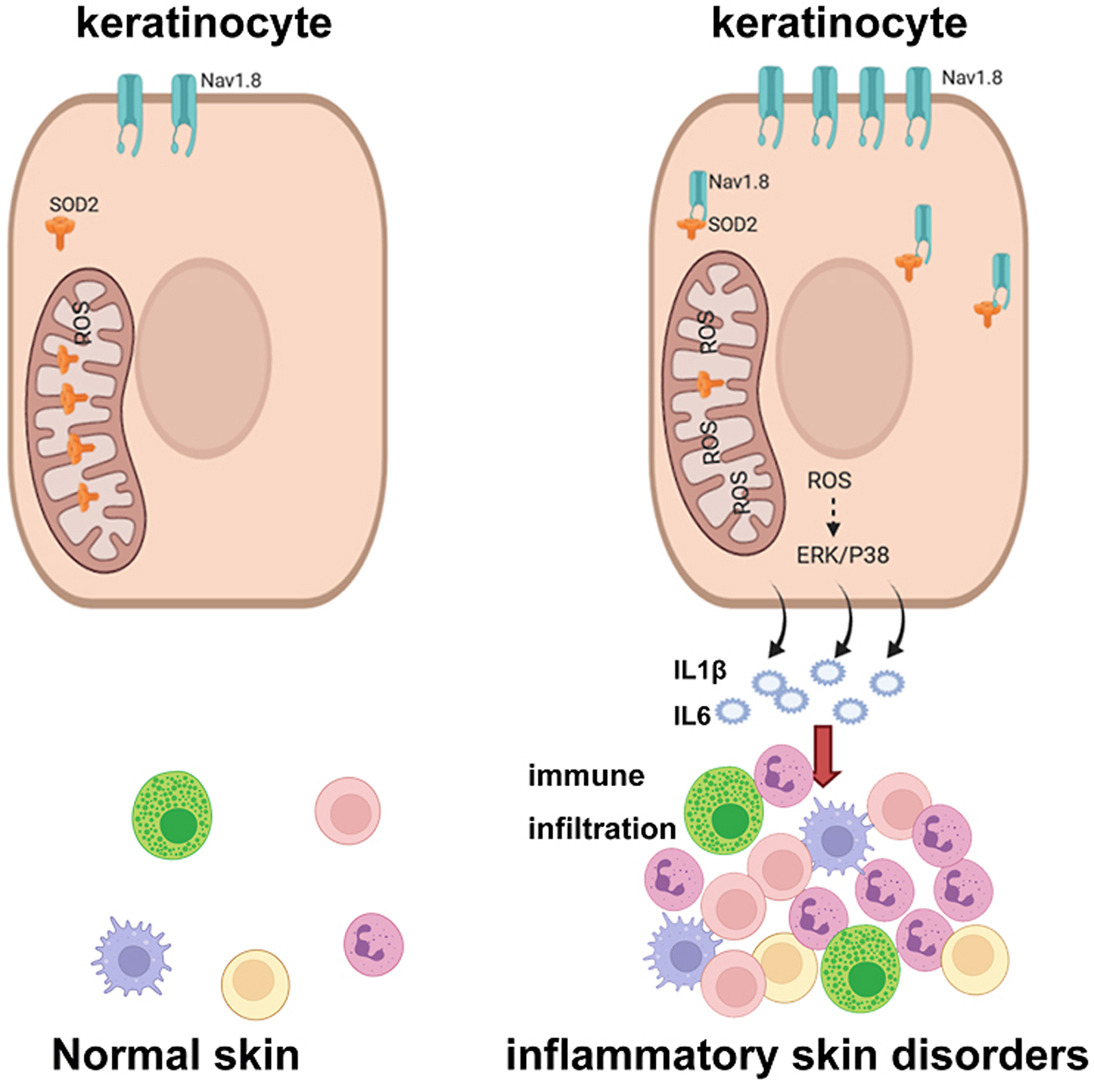
在遗传学层面,玫瑰痤疮家系全基因组测序发现 LRRC4、SH3PXD2A 和 SLC26A8 的罕见变异均涉及神经突触相关通路,导致神经肽过度释放(Nat Commun 2023)。血清蛋白质组学进一步解析出炎症主导型和神经源性-代谢型两种分子亚型,为个性化治疗提供了分子基础(JAAD 2026)。STAT3/IL-36G(J Adv Res 2025)、KRT6A/JAK1-STAT3(J Biomed Sci 2025)及 Nav1.8 介导的 ROS 信号通路(Redox Biol 2022)等关键炎症通路均已系统阐明,新型纳米酶 ROS 清除剂则为治疗提供了新思路(Redox Biol 2024)。
基于上述机制研究,相关干预策略已在多中心随机对照试验中得到验证,并逐步应用于临床。研究证实加巴喷丁可有效改善玫瑰痤疮潮红(JAAD 2025),帕罗西汀可有效治疗难治性红斑(JAAD 2023),羟氯喹可安全有效地治疗玫瑰痤疮(JAAD 2021)。
毛发疾病与再生
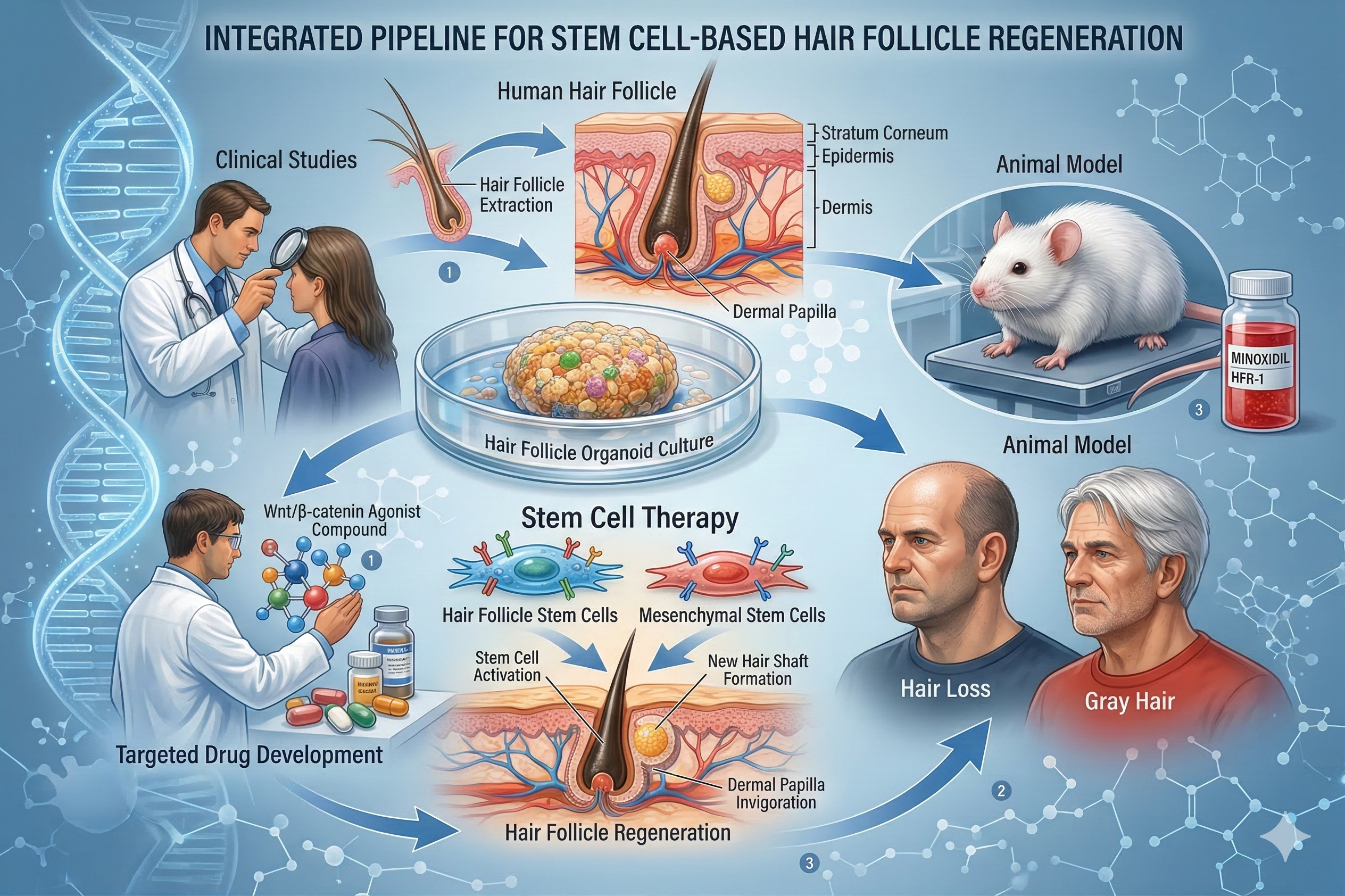
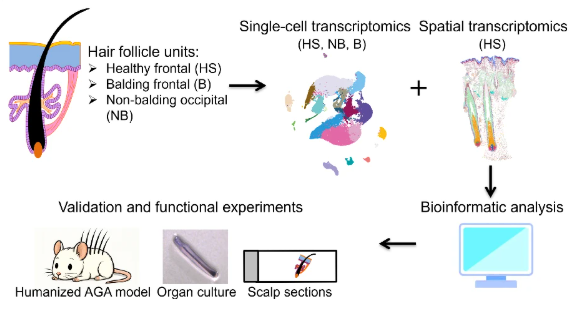
雄激素性秃发(AGA)表现为毛囊渐进性微型化,但介导毛囊微型化的分子机制尚不清楚。团队构建的人类 AGA 生长期毛囊单细胞转录组图谱揭示,结缔组织鞘(CTS)过度收缩激活机械敏感通道 PIEZO1,诱导毛囊祖细胞异位凋亡,促进毛囊微型化进程。MLCK 抑制剂 ML-7 在患者来源的离体模型和人源化小鼠中均可恢复毛发生长(Nat Commun 2026)。
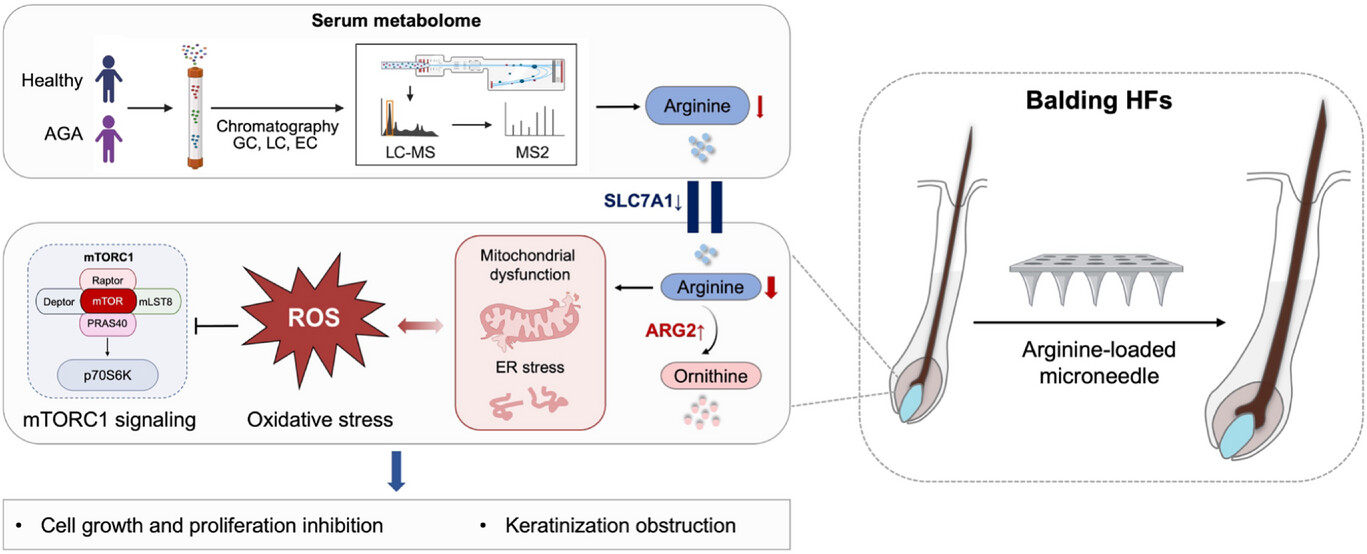
代谢谱分析进一步发现精氨酸代谢紊乱在 AGA 发病中发挥关键作用:转运体 SLC7A1 下调与 ARG2 上调导致 ROS 蓄积和 mTOR 失活,微针递送精氨酸方案可恢复毛发生长(Adv Sci 2025)。
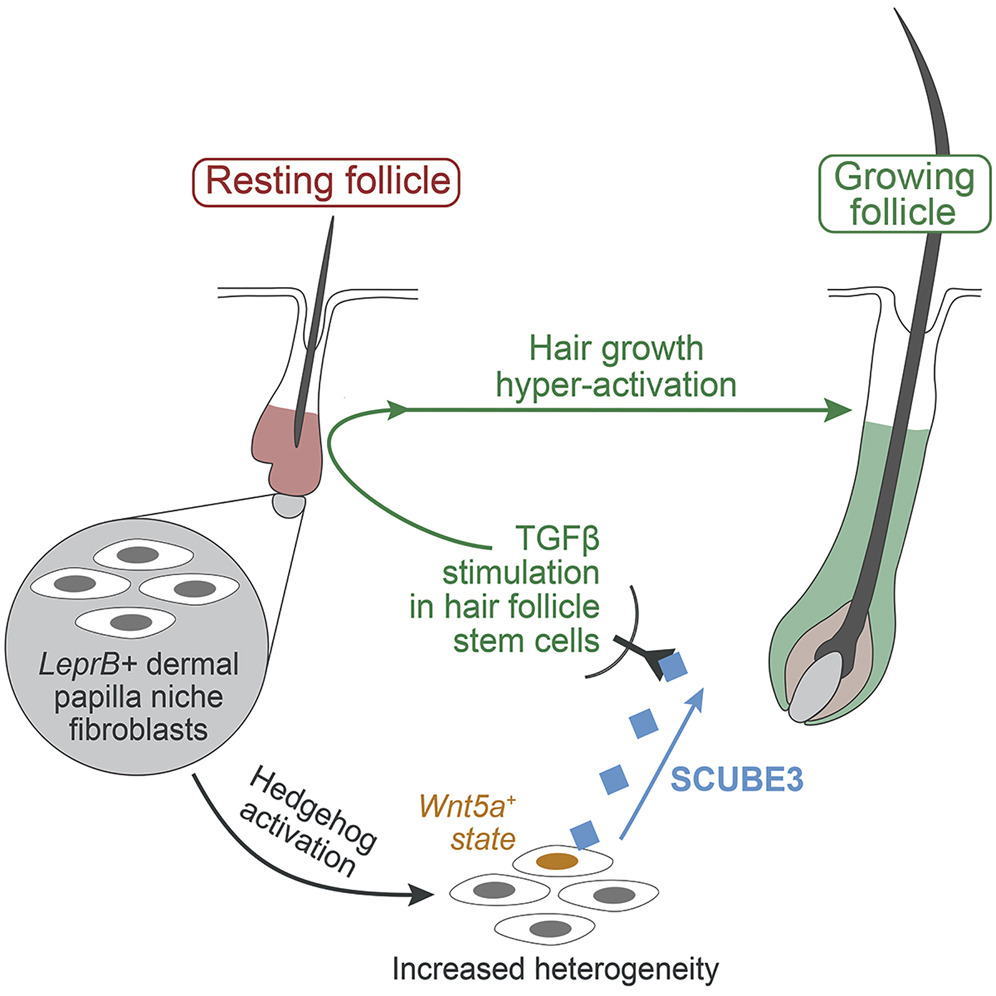
在毛发色素研究中,利用黑素前体细胞构建的皮肤类器官揭示了色素模式建立的两步调控机制:体外培养阶段 COL6A3-CD44 信号维持类器官中的黑素细胞,移植后形态发生阶段 SEMA3C-NRP1 信号引导其迁移至隆突干细胞龛(Adv Sci 2025)。在毛囊再生研究中,团队发现毛乳头微环境中 Hedgehog 信号过度激活可重编程周围成纤维细胞产生 SCUBE3(一种 TGF-β 配体),足以诱导新毛发生长(Dev Cell 2022)。
针对斑秃,一系列真实世界临床研究建立了基于 JAK 抑制剂的管理策略:利特昔替尼在不同解剖部位、青少年群体及既往 JAK 抑制剂难治患者中均展现出显著疗效,托法替尼的个体化减量方案可在不影响疗效的前提下维持治疗应答(JAAD 2025;JAAD 2026;JAAD 2026;J Cutan Med Surg 2026)。
皮肤衰老
衰老是涉及全身各个器官系统的复杂多因素生物学过程。皮肤因其直观性和易获取性,是研究衰老生物学的理想模型。实验室综合运用长寿人群队列、多组学技术及细胞与动物模型,系统研究皮肤衰老的核心机制。
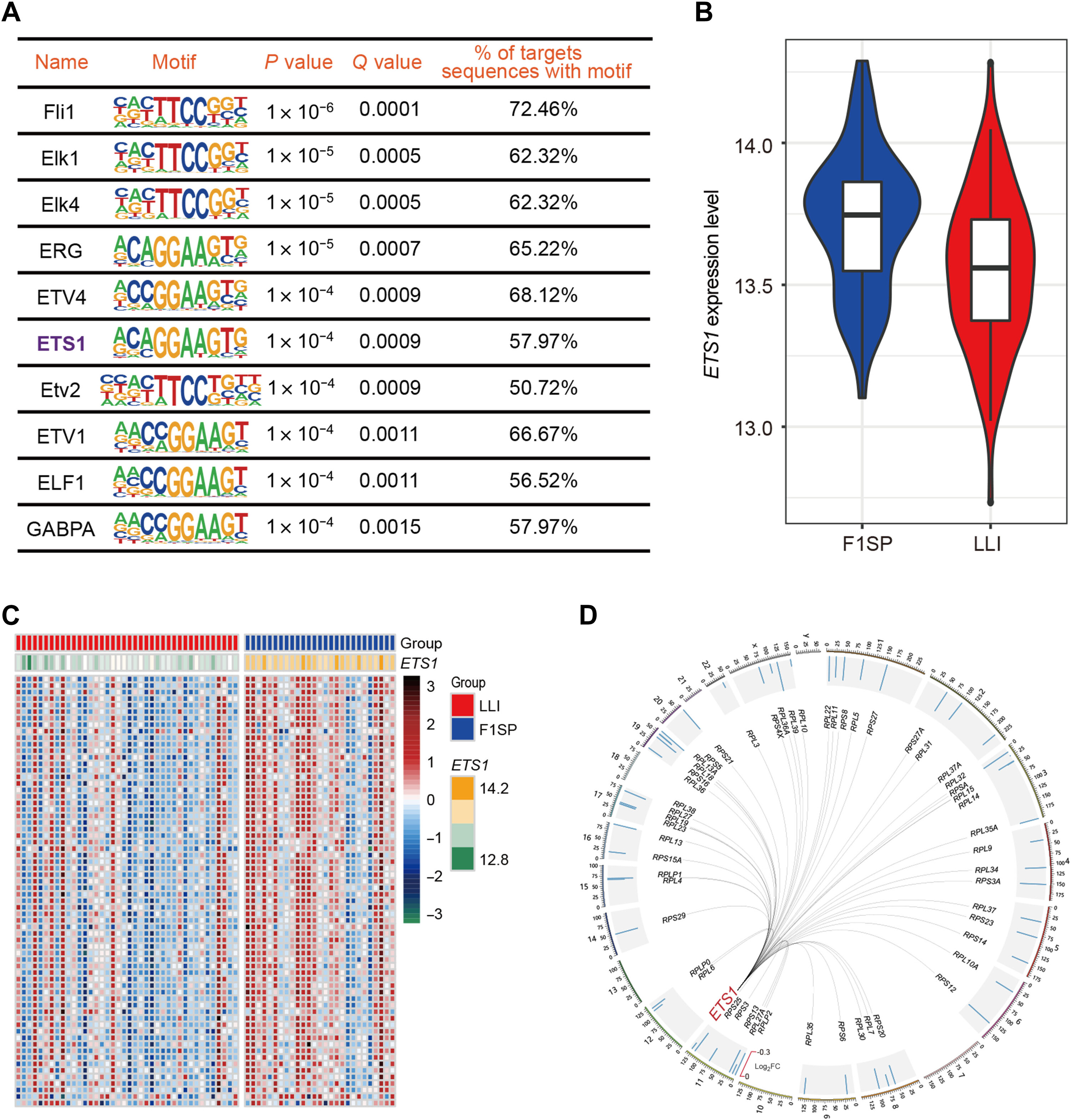
实验室是衰老生物标志物联盟(Aging Biomarker Consortium)的核心成员,该联盟旨在建立中国跨器官系统的标准化衰老生物标志物体系(Nat Med 2023)。基于长寿队列转录组学分析,团队发现 ETS1 通过下调核糖体蛋白基因表达抑制高能耗的核糖体生物合成过程,提示核糖体生物合成的下调可能是长寿人群适应性能量代谢调控的关键环节(Sci Adv 2022)。
在表观遗传水平,团队发现 m6A 去甲基化酶 FTO 缺失可通过 KAT8/RSF1 乙酰化级联反应导致异染色质丢失,为 RNA m⁶A 修饰参与皮肤衰老过程中的染色质重塑提供了新证据(MedComm 2025)。在转录因子调控网络方面,HOXC10 通过 FZD6/Wnt/β-catenin 通路延缓成纤维细胞衰老,经 Connectivity Map 筛选发现辛伐他汀可作为其功能类似物(Research 2025)。
上述基础发现正推动抗衰老药物的合理设计,最终目标是将来自长寿人群研究和细胞衰老机制的分子发现转化为有效的临床干预策略。